Esta combinación acaba con la resistencia del cáncer a la inmunoterapia
La inmunoterapia es una forma de tratar el cáncer reprogramando el sistema inmunitario del paciente para que ataque su tumor. Este enfoque de vanguardia ha tenido un impacto significativo en el tratamiento de los pacientes con cáncer, y ya cuenta con casos de remisión a largo plazo.
Sin embargo, muchos pacientes siguen sin responder a la inmunoterapia o, si lo hacen, los efectos son temporales, lo que pone de relieve la importancia de comprender mejor los mecanismos que hacen que los cánceres se resistan a este tipo de tratamiento.
El cáncer neuroendocrino de páncreas es muy resistente a un tipo de inmunoterapia denominada bloqueo de puntos de control, en la que el paciente recibe un fármaco (un inhibidor de puntos de control) que bloquea proteínas que normalmente impiden que las respuestas inmunitarias sean demasiado fuertes, pero que también pueden impedir que las células inmunitarias (células T) eliminen las células cancerosas.
El estudio fue dirigido por el grupo de Douglas Hanahan, del Instituto Suizo de Investigación Experimental del Cáncer de la EPFL, con el Instituto Ludwig de Investigación Oncológica, el Hospital Universitario de Lausana (CHUV), el Instituto Suizo de Bioinformática y Roche.
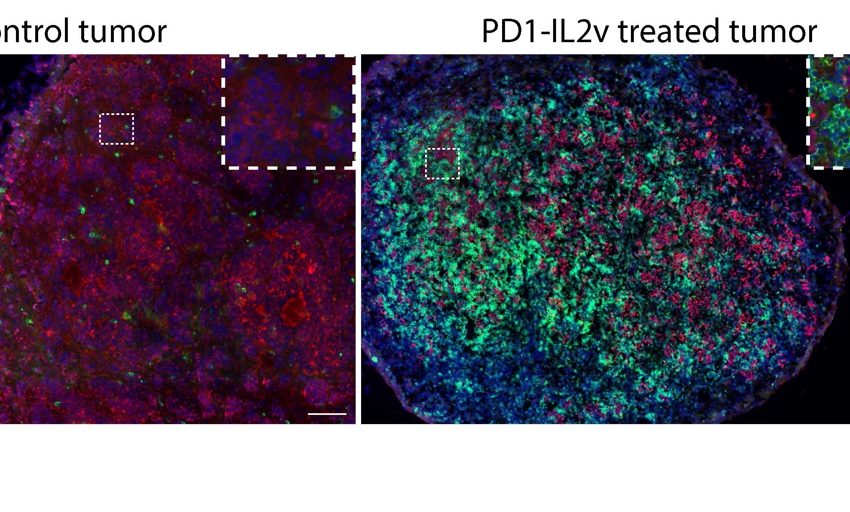
Los científicos evaluaron un tipo de fusión proteína-anticuerpo denominada inmunocitoquina, cada vez más utilizada en inmunoterapia. Se centraron en la inmunocitoquina biespecífica PD1-IL2v, desarrollada recientemente por Roche y capaz de introducirse en los tumores, donde activa las células T asesinas para que ataquen a las células cancerosas que impulsan el crecimiento tumoral.
Los investigadores combinaron la inmunocitoquina PD1-IL2v con el inhibidor del punto de control inmunitario anti-PD-L1, potenciando así la inmunidad antitumoral contra los tumores resistentes a la inmunoterapia. «La [PD1-IL2v] es aún más eficaz cuando se combina con un inhibidor del punto de control inmunitario, el anti-PD-L1», escriben los autores.
«PD1-IL2v induce una expansión más fuerte y específica de las células T antitumorales en comparación con la terapia anti-PD-1 convencional mediante la estimulación de un subtipo específico de células T, mientras que anti-PD-L1 se dirige e interrumpe las barreras erigidas en el microambiente tumoral, a saber, los macrófagos pro-tumorales y la vasculatura tumoral, que colaboran para contrarrestar la inmunidad antitumoral».
La combinación de las dos moléculas dio lugar a un aumento de la tasa de supervivencia en ratones portadores de tumores, produciendo un efecto terapéutico más sostenido que la inmunocitoquina biespecífica por sí sola. La combinación mejoró la eficacia terapéutica al reprogramar los macrófagos inmunosupresores asociados al tumor y la vasculatura tumoral para que el cáncer fuera más fácil de «detectar» por las células inmunitarias.
«Esta innovadora combinación inmunoterapéutica sensibiliza a los tumores resistentes a la inmunoterapia infiltrados con linfocitos T tipo PD-1+, que recientemente se han revelado importantes para mantener respuestas inmunitarias antitumorales eficaces, lo que conduce a la destrucción del tumor con el consiguiente beneficio para la supervivencia y concluye: «Estos resultados provocativos presentan una justificación para los ensayos clínicos destinados a evaluar la terapia combinada de PD1-IL2v y anti-PD-L1, tal vez inicialmente en pacientes con cáncer resistentes a la inmunoterapia con tumores infiltrados por células T».
Fuente de la noticia: Pulsa para ver la noticia en el periódico que ha sido publicada.
(Salamanca Realidad Actual es un lector de noticias FEED que unifica las noticias de diferentes periódicos sobre Salamanca. No hemos redactado ninguna de las noticias aquí publicadas y la totalidad de el copyright de esta noticia pertenece a: www.abc.es y (abc) ).